23 Mars -
Pénuries de médicaments : les pharmaciens hospitaliers peuvent jouer un rôle clé dans le maintien de l'approvisionnement, conclut un rapport Amgen lors du congrès 2012 de l'EAHP - Le rôle des pharmaciens hospitaliers est essentiel au maintien d'un approvisionnement continu en médicaments lorsque les pénuries mettent en danger la vie des patients, a révélé un rapport
Amgen ((1) : Mica, A. & Green, L. Drug availability: considerations for the hospital pharmacist (Disponibilité des médicaments : Considérations pour les pharmaciens hospitaliers)) lors du congrès annuel 2012 de l'
Association européenne de pharmacie hospitalière (EAHP), qui a eu lieu à Milan, en Italie.
« Les pénuries de médicaments, en particulier les traitements en oncologie, constituent un problème croissant à travers l'Europe, » a expliqué Richard Lit, vice-président Regulatory Affairs and Safety (affaires réglementaires et sécurité). « Plusieurs rapports indiquent que des pays comme l'Allemagne, la Hongrie, les Pays-Bas et le Royaume-Uni(
2) souffrent de pénuries de médicaments brevetés(
3), biosimilaires, et génériques, qui causent des problèmes pour les patients, les prescripteurs et les pharmaciens. »
« Devant l'incapacité d'accéder au médicament choisi, les médecins et les pharmaciens hospitaliers sont contraints de faire des compromis, en recourant à d'autres médicaments, en rationnant, voire en reportant les traitements critiques. Il est inacceptable que les patients soient privés de traitements éprouvés ou choisis à cause de problèmes évitables dans la chaîne d'approvisionnement, » a-t-il ajouté.
Sur l'affichage présenté au congrès de l'EAHP
(Drug Availability: Considerations for the Hospital Pharmacist (Disponibilité des médicaments: Considérations pour les pharmaciens hospitaliers), les auteurs font référence aux médicaments « biologiques » (des médicaments fabriqués aux moyen de processus biologiques) en tant qu'exemple illustrant la manière dont les pharmaciens peuvent utiliser les paramètres de la chaîne d'approvisionnement afin de mieux identifier les fabricants capables de maintenir un approvisionnement continu en médicaments.
Les pénuries de médicaments se produisent pour un certain nombre de raisons, parmi lesquelles la rareté des matières premières, les arrêts d'exploitation dus à des contaminations de gammes, les rappels volontaires et les changements de composition. De plus, la pratique des appels d'offres, dans le cadre desquels les hôpitaux concluent des contrats avec la société pharmaceutique proposant la meilleure offre, est susceptible d'exacerber le problème en transférant le volume demandé d'un fabricant à un autre - entraînant des pénuries temporaires.(
4)
En Europe, les fabricants sont tenus d'informer l'
Agence européenne des médicaments, par préavis de deux mois, de l'éventualité d'une interruption temporaire ou permanente de l'approvisionnement d'un produit.
((5) Directive 2001/83/EC du Parlement européen et du Conseil du 6 novembre 2001 dans le code de la Communauté sur les produits médicaux destinés à l'utilisation humaine (OJ L 311, 28.11.2001, p. 67). Bruxelles : Commission européenne ; 2001) Aux États-Unis, il n'existe aucune loi exigeant des fabricants qu'il signalent les pénuries.(
6) Les agences de régulation tentent de développer un certain nombre de processus en la matière, mais bien que ceux-ci contribuent à une gestion des pénuries, ils ne sauraient les empêcher.(1)
En évaluant la manière dont un fabricant gère son approvisionnement en médicaments, les pharmaciens peuvent prendre des décisions considérées comme formulaires, qui maximiseront leurs chances d'approvisionnement constant en médicaments.
Les pratiques suivantes améliorent la capacité des fabricants de produits fabriqués par processus biologiques à maintenir une production ininterrompue et continue de l'approvisionnement :(1)
- Une liaison entre la demande des patients et la production, au travers de systèmes d'information intégrés sur la fabrication et la distribution
- Un système de double fournisseur s'agissant du sourçage de matières premières, et un recours à des fournisseurs certifiés
- Le maintien de stocks de sécurité afin de compenser les éventuels retards et interruptions de fabrication
- Une gestion stratégique de la capacité, et la possibilité de capacités excédentaires de fabrication afin de contrer tout retard de production
- Une gestion active de réseaux de distribution solides et sécurisés - un réseau de distribution de société pharmaceutique s'occupant de déplacer les produits qui nécessitent d'être conservés en sécurité
« L'accès à des médicaments efficaces et de haute qualité est indispensable au succès de la gestion médicale, » a commenté Richard Lit. « En prenant ces facteurs en considération au cours d'une évaluation approfondie du fournisseur potentiel, les pharmaciens hospitaliers peuvent augmenter leurs chances d'éviter les pénuries de médicaments essentiels, » a-t-il ajouté.
À propos des médicaments biologiques
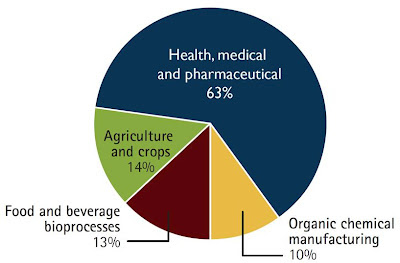
Les médicaments biologiques sont fabriqués à base d'organismes vivants et de substances organiques, et comprennent les protéines thérapeutiques, les vaccins à ADN, les anticorps monoclonaux et les protéines de fusion, de même que les nouvelles modalités expérimentales de type thérapie génique, thérapie par cellules souches, nucléotides antisens, et virus à ARN. Ils sont fabriqués en utilisant des cellules vivantes pour produire des protéines qui peuvent être utilisées afin de traiter la maladie. En exploitant le processus naturel des cellules, virus et autres organismes microscopiques vivants, les scientifiques modifient le patrimoine génétique des organismes dans le but d'en tirer des résultats spécifiques.
Contrairement aux médicaments à petites molécules, les produits biologiques sont généralement des protéines fabriquées dans des cellules vivantes génétiquement modifiées, dans lesquelles la moindre variation de cellule, de ses nutriments ou de l'environnement peut entraîner des différences dans le produit final.
À propos des médicaments biosimilaires
Les médicaments biosimilaires sont des copies similaires des médicaments biologiques novateurs. La substance active d'un médicament biosimilaire est similaire au médicament original de référence mais, en raison des complexités de la fabrication biologique, il n'est pas possible pour un biosimilaire d'être une copie exacte du produit original.
Lorsque le brevet d'un médicament expire, les autres fabricants ont la possibilité d'en faire des copies. Dans le cas des médicaments à petites molécules, les tests d'analyse peuvent démontrer une équivalence pharmaceutique au produit novateur. En revanche, s'agissant des médicaments biologiques (médicaments à grosses molécules), une gamme d'études analytiques, cliniques et non cliniques ne peut révéler qu'une similarité et non un caractère identique. Ceci s'explique par les structures complexes des produits biologiques, l'utilisation de cellules différentes, et les procédés de fabrication distincts...
lire la fin du communqiué de presse Amgen -